在制药行业,人们的目光总会聚集在一些重磅药物上,如 礼来的替尔泊肽,诺和诺德的司美格鲁肽、亦或是默沙东的K药……这些名字常年霸榜头条,光环耀眼。但聚光灯之外,还有几十上百款老药,依然在稳稳地为各大药企贡献着收入。它们或许不够出挑,却是账面上实打实的现金牛。然而每年都有一批这样的成熟产品迎来专利到期。
$ I/ U( K" U% C& |& d8 q近日,Fierce Pharma发布报告,2026年将有10款重磅药物失去美国独占权,这些药加起来年销售额超过130亿美元。从常年畅销的抗过敏药,到肿瘤治疗的基础用药;从自身免疫疾病的核心品种,到针对罕见病的孤儿药——它们的专利到期,影响的远不止是原研药企的财报,还有这些治疗领域的市场格局,这也是仿制药领域玩家的一个重大机遇。
/ e9 E: Z2 ~" I; T* B) z9 z
/ s5 ]& v% }! l01, s* H/ L# @) [' }! H$ k$ s
罗氏/Xolair(奥马珠单抗)% A5 j; [3 J/ ^4 o* c J
适应症:哮喘、慢性特发性荨麻疹、慢性鼻窦炎伴鼻息肉、食物过敏
' u9 D6 L5 q2 k2 `/ @# w2025年美国销售额:约37亿美元(30.8亿瑞士法郎)
) d! o5 ^+ `4 l3 ]6 x: Q随着Xolair在美国的最后一项专利到期,这款来自罗氏的免疫学老将,结束了其在美国长达二十多年的市场独占时代。尽管主要专利在2010年代末就已过期,但凭借预充式注射器剂型的获批,Xolair的保护期得以延长了数年。
7 b& |+ y3 b$ O: t& Y0 y2 i# U6 b罗氏预计, 其生物类似药将于2026年下半年在美国上市。即便如此,这款单抗药物 去年在美国依然卖出了约30.8亿瑞士法郎(约37亿美元),较前年猛增32%,也助推罗氏在美国的整体销售额增长了8%。
3 B7 W: F+ d% i8 T aXolair最初于2003年在美国获批,由罗氏子公司基因泰克研发,并一直与诺华合作,由后者负责美国以外的市场。 Pharma ONE药物研发大数据平台显示,迄今为止, 仅有韩国Celltrion一家公司的Xolair生物类似药获得了FDA的批准,并覆盖Xolair全部四项适应症。
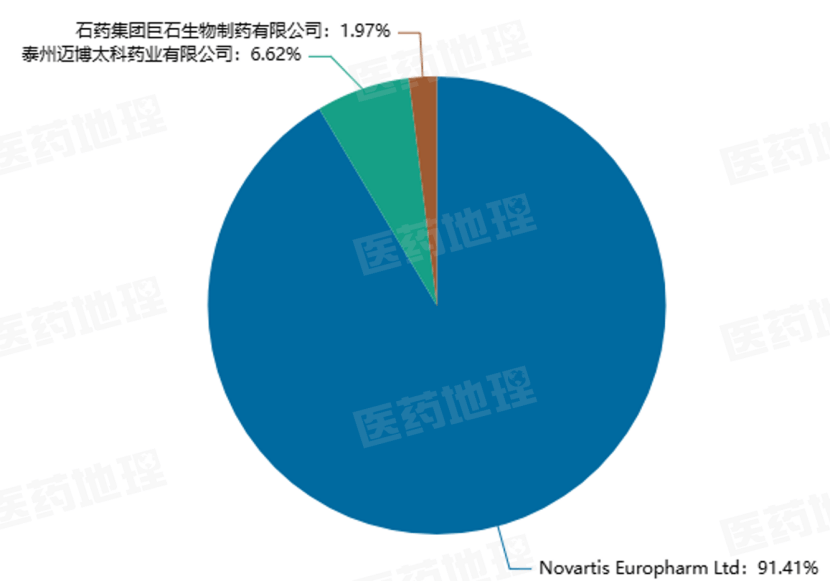
' ~& E% j" t$ E# _而在中国,已有泰州迈博太科药业和石药集团巨石生物两家的奥马珠单抗获批上市。 PDB药物综合数据库显示,2025年该药在国内院端市场中, 原研药仍牢牢占据90%以上的销售份额。
/ E, s3 |7 F- K; l) N! l) r; f- n
 $ }! l3 W* V( j$ T
$ }! l3 W* V( j$ T
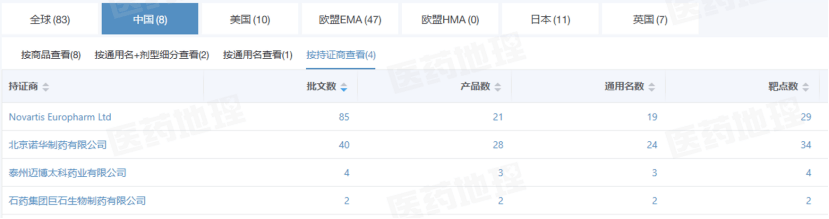
* V7 F% ~; M5 ^9 j9 R0 w6 ?. `奥马珠单抗全球获批情况 * ]' h% ^( U* J* z
来源:Pharma ONE药物研发大数据平台,中国医药工业信息中心
& u0 i' t$ V1 G8 F7 S0 y0 p0 \
 5 d# f$ E7 S& k- A" l
5 d# f$ E7 S& k- A" l
奥马珠单抗国内院端销售份额(2025)
! i( E2 E7 y: U. u来源:PDB药物综合数据库,中国医药工业信息中心
" f0 h- s4 Q0 O4 a. f) W02
. K) Z& h" \7 S1 F. i3 ? I百时美施贵宝/Pomalyst(泊马度胺)
& D0 I/ n' m1 o. o( u5 C! ]适应症:多发性骨髓瘤、卡波西肉瘤
+ ]) D/ E3 f' {$ s2025年美国销售额:23.4亿美元 3 c" A. t: D9 o6 Z. O0 \1 P/ H
百时美施贵宝在发布四季度财报时,其中一个核心主题便是多款重磅药品正面临专利保护到期的挑战。 血癌药物Revlimid和Sprycel的销量持续下滑且这两款药物分别于2022年和2024年失去专利独占权。未来几年, 抗凝药Eliquis和抗癌药Opdivo的专利保护也将陆续到期,而这对组合去年全球销售额总计达245亿美元,占公司总收入的51%。 , N5 a& ~ @, ]% ]$ o. p% [
不仅如此,BMS还即将遭遇美国市场针对Pomalyst(波马度胺)的仿制药竞争。目前, 该药在欧洲已因专利失效而销售额下滑,从2024年的35.5亿美元降至去年的27.3亿美元。BMS在上月的一份监管文件中表示,美国市场的仿制药预计将于2026年第一季度开始冲击。
: L) o C% ~. nPomalyst最初由Celgene开发,于2013年获得FDA批准,上市第三年便成为重磅产品。三年后,BMS以740亿美元收购了Celgene。进入本世纪20年代,随着市场竞争日趋白热化,尤其是强生的重磅药物Darzalex(去年销售额高达144亿美元)的强势表现,Pomalyst的销售增长放缓并陷入停滞。为延长Pomalyst的专利寿命,BMS曾针对包括Dr. Reddy's、Natco、梯瓦在内的多家仿制药厂商提起侵权诉讼,最终都以和解告终,各方同意将仿制药上市时间推迟到2026年。
, X/ e! j! R- A2 ~9 q目前, 梯瓦、Apotex、Hetero、Breckenridge以及印度Aurobindo的子公司Eugia,都已获得FDA对Pomalyst仿制药的批准。 3 R( s+ X* l5 t
03* u1 u- B; ~: ?/ f, O& Z3 w$ |
强生/Opsumit(马西替坦)9 O* c5 D& p) q" j6 ]& ~6 _0 z$ d
适应症:肺动脉高压 3 _, Y; D2 c3 g! J
2025年美国销售额:16.3亿美元
; k& U# R7 x: \继2025年重磅药物Stelara因专利到期销售额锐减后,强生2026年将面临另一款肺动脉高压药物Opsumit的仿制药冲击。Opsumit是强生2017年以300亿美元收购瑞士Actelion公司获得,一直是其罕见病业务的重要支柱。尽管面临新一代药物如默沙东Winrevair的竞争, Opsumit 2025年全球销售额仍达23.2亿美元。) k0 K$ [' J! q7 K$ [/ J% }% E
目前已有10家公司获FDA批准生产Opsumit的仿制药。FDA橙皮书显示,该品牌药的一项关键专利将于今年6月到期。强生首席财务官已明确表示, Opsumit预计2026年将开始受到仿制药影响。) h/ j5 F& T: y/ M. ]
04. w- t4 b4 D8 ?
默沙东/Januvia/Janumet(西格列汀/西格列汀二甲双胍)
- k: C# b( Q% W# n# {/ H9 g适应症:2型糖尿病 # g9 ?1 h s4 z" W" [1 z4 ]
2025年美国销售额:12.7亿美元 7 F# G* t: k" ]5 w( J% ?
默沙东的经典糖尿病药物Januvia和Janumet在美国的专利保护也将在2026年走向终点。 尽管核心成分专利早在2023年就已到期,但另一项涵盖特定盐形式的专利将保护期延长至2026年,其中缓释版Janumet XR的独占期预计能到今年7月。
: K$ B0 N2 T; W默沙东已与至少25家仿制药公司达成和解,允许其仿制药在2026年5月后上市。然而Viatris则另辟蹊径,没有一开始就寻求和解,而是试图在法庭上挑战默沙东的专利。有趣的是,在2022年,这一计划反而帮了默沙东一把。西弗吉尼亚州一家联邦法院判决,Viatris挑战的两项默沙东专利有效,且Viatris推进仿制药的行为构成侵权。直到2023年3月,Viatris才松口,与默沙东达成了一项保密和解。当时双方表示,协议允许Viatris在"相关诉讼专利到期前的特定日期"销售其仿制药。
- _, m( V* X6 o$ g+ h$ F- A5 a2 R% p这意味着,这款曾经的“印钞机”在美国市场的销售额将“大幅”下降。 2025年,该药物组合在美国销售额约12.7亿美元,全球销售额为25.4亿美元,后者较前一年下降了12%。
$ {' ^. g/ l" U9 m9 h5 _5 o05
) Q, G3 g3 b' `强生/Simponi(戈利木单抗)) ]% @9 o1 j5 R, X. |
适应症:溃疡性结肠炎、强直性脊柱炎、银屑病关节炎、类风湿关节炎 ; w. a3 w: G/ [( U5 p1 o
2025年美国销售额:11.9亿美元
- P9 ?3 \$ D* R) z6 O& u强生的另一款TNF抑制剂Simponi也将在2026年面临生物类似药的竞争。其物质成分专利已于2024年到期,这个专利悬崖的时间点与强生的另一款免疫学重磅药物Stelara高度重合。% |+ Z/ l t( s4 q. t" o) }
尽管Simponi的生物类似药赛道没有Stelara那么拥挤,但仿制药一旦登场,挑战同样不容小觑。 Simponi及其静脉输注版本Simponi Aria去年的全球销售额总计27亿美元,比2024年增长了21.8%。; S% Q1 k& a% G3 W- r. J( [
去年,Alvotech的仿制药因生产缺陷在美国上市遇阻,但Simponi生物类似药却已以Gobivaz的名字在欧洲上市,由Advanz Pharma负责销售。Alvotech本打算在上市后"独享"欧洲市场"几个月",但Bio-Thera及其欧洲合作伙伴Stada已紧追不舍。 Bio-Thera的仿制药Gotenfia于2月获得了欧盟委员会批准,适应症与原研药一致,正准备"在未来数周或数月内"上市。
3 y) R. x# p. }与此同时,强生也在密切关注着对手的动向。 公司表示,美国的Simponi仿制药预计会在今年下半年出现。7 o6 @ D) p! E) J
06* m9 g- S+ U& q# V; {
默克/Mavenclad(克拉屈滨)
$ {7 X/ b+ V7 I0 N适应症:复发型多发性硬化症 7 f! c) M9 C' f/ r# C7 y4 M
2025年北美销售额:7.16亿美元(6.35亿欧元)
9 G. t( ?8 ^; i: C3 ^与其他“老药”不同,德国默克公司的Mavenclad上市时间并不长,自七年前上市以来,它迅速跨越了重磅炸弹的门槛,成为公司的创收主力。 2025年,该药全球销售额为11.9亿欧元,但其专利保护期却将结束。去年10月的一项法院判决认定Mavenclad的两项专利无效,这为更多仿制药厂商的入局打开了大门。
/ [" Q& P! C% H目前加拿大仿制药商Apotex已获得Mavenclad仿制药的批准,Hopewell Pharma Ventures也获得了暂时批准。默克在财报中表示,从2026年3月起,其业绩指引中将不再计入Mavenclad的未来销售额,并预计这款药物的专利悬崖将导致其医疗保健业务板块在2026年整体下滑。
- R, n- ]; O# h$ f" e, L07
3 B& F9 Y4 t. D1 S武田/Gattex(替度鲁肽)6 P% o; Z9 {$ E4 } b: T% o+ f
适应症:短肠综合征
, w5 p G3 G" z- I. I2 f: J$ d2025年美国销售额:约7.07亿美元(1058亿日元)
7 i3 c2 M5 |4 ^. I6 h作为唯一获批治疗短肠综合征的药物,Gattex一直是武田稳定的销售来源。这款GLP-2类似物自2019年武田收购夏尔(耗资620亿美元)获得,其儿科独占权将持续到2026年5月16日,但仿制药进入美国市场的确切时间仍是未知数。
" E$ e) @+ C# l6 z潜在的仿制药竞争者之一是Cipla和Orbicular Pharmaceutical Technologies,英国药品目录中已出现Cipla的替度鲁肽仿制药标签,而Viatris生产的Gattex仿制药则在今年1月获得了欧洲监管机构的批准。( T, L- A) `' a s* L
08/ _1 ~ V6 }) B7 P# [5 `
武田/Trintellix(伏硫西汀)8 a; {8 P- T/ N8 g6 O1 ^9 v
适应症:重度抑郁症 1 Q+ J& [$ k7 G7 k* j, j: V
2025年美国销售额:约6.98亿美元(1046亿日元) 7 A4 w4 E* q$ s r D
在经历了ADHD药物Vyvanse的专利悬崖后,武田将在2026年面临另一款药物Trintellix的活性成分于2026年12月的专利到期, 该药2025年在美国的销售额为1046亿日元。* r& V9 h' g! ?7 z
面对即将到来的仿制药冲击,武田与其长期合作伙伴灵北近年来已采取多项措施,提前调整业务布局。今年1月,武田宣布将在美国近50个州裁员200多人,作为其神经科学业务重组的一部分。而在一年前,武田刚从灵北手中完全接过了Trintellix在美国的销售权。
+ Q0 D& v+ e5 z$ g. C09% M& S. y6 D8 D* Z: I E
优时比/Briviact(布瓦西坦)/ @' w* w @4 @* W! \+ F
适应症:癫痫 . k( t# D. t2 ?& k4 o: Z1 ^3 l
2025年美国销售额:约6.52亿美元(5.78亿欧元)
3 [. v- ]* S! P% A优时比的抗癫痫药物Briviact在美国的独占期已于2026年2月结束,欧洲市场也将在8月面临仿制药竞争。 2025年全年,Briviact的全球销售额达到7.58亿欧元(约8.55亿美元),比2024年增长了11%。! X% F& g& ]8 _: v! b' @" w$ M( w4 a
就在2月的最后一周, 印度Lupin公司已率先在美国推出其口服溶液仿制药。. D3 J" R) x( h5 X2 ^9 D
尽管面临专利失效,优时比旗下新上市的产品阵容足以轻松对冲今年仿制药的影响。在2月发布的2026年业绩指引中,优时比预计, 像Bimzelx、Rystiggo、Zilbrysq、Fintepla和Evenity这些药物的持续增长,将"超额弥补" Briviact在欧美失去独家权而导致的预期净销售额下降。) B! G. T2 U; p7 ^* Q
与此同时,优时比在癫痫领域的布局也未停歇。2022年,公司以19亿美元收购了罕见病药企Zogenix,从而获得了Fintepla。该药于2020年获批治疗与罕见癫痫类型Dravet综合征相关的癫痫发作,并在同年也获批用于Lennox-Gastaut综合征。
. Z8 j! x1 t0 ]; h10- } _6 N3 M! Y# C
辉瑞/Xeljanz(托法替布)
+ y8 M0 D0 D1 M9 g) e% q3 m适应症:类风湿关节炎、银屑病关节炎、幼年特发性关节炎、溃疡性结肠炎、强直性脊柱炎 % {7 K+ ?2 x( ?
2025年美国销售额:6.25亿美元 2 u- j" P% |& l( H
在以上盘点的专利失效TOP10药物中,多数产品的销售额都是在面临仿制药竞争的前一年达到顶峰。 但Xeljanz是个例外,它的全球收入峰值早在2021年(24.5亿美元)就已出现,此后便一路下滑,去年已跌至10.9亿美元。- h: m. C) s0 X3 L; J
原因何在?首先,2021年FDA给所有JAK抑制剂类药物的标签上都加上了黑框警告。作为最早上市的JAK抑制剂之一,也是首个获批用于类风湿关节炎的JAK抑制剂, Xeljanz首当其冲,遭受重创。6 J5 B+ i* j; D8 V
其次,其他疗法的有效性也对Xeljanz构成了挑战,比如艾伯维的Rinvoq。Rinvoq同样属于JAK抑制剂,但因其对JAK酶更具选择性的抑制作用,被视为更安全的选择。
1 Q0 k7 y/ v. T3 ~% i5 D不过,与即将面临的专利失效相比,Xeljanz的下滑对辉瑞来说可能只是小巫见大巫。其另外几款重磅药物——Ibrance、与BMS合作的Eliquis、与安斯泰来合作的Xtandi——都将在2027年底前失去美国专利保护。 这三款药物去年的全球销售额合计超过140亿美元。8 v& m/ I- {" H0 G# V
根据FDA橙皮书, 目前已有八家公司的Xeljanz仿制药在美国获批。据相关机构估计,仿制药上市后,Xeljanz的价格有望从目前的每片80美元降至10至20美元之间。
' X) ~6 V. [! C( H& E; m! O结语! y0 X- o) u! u5 h% e
在医药行业的历史长河中,每一款重磅药物的诞生,都是一段科学探索与商业智慧交织的传奇。 它们曾为无数患者带去希望,为研发企业筑起高墙,也支撑起一个时代的治疗格局。
' o# S( n; s, R然而,专利的到期,既是终结,也是开端。正是这种 “创造—独占—竞争—再创造”的节奏,推动着整个行业不断向前。失去独占权的同时,也为新一代药物腾出了市场空间,为新锐企业提供了入场券,更为全球患者带来了更可负担的治疗选择。 & c: M) c, p" J4 s- j& W
互动投票 |