|
|

9 i3 q: u: g! l5 D* E# V
" Y/ {( H5 m$ r& o2 _+ z9 n1 X2026年3月12日,山东第二医科大学基础医学院于博文、梁淑娟课题组于Nature Communications杂志在线发表了题目为
0 V6 s5 \! q! U6 S. H' o8 @- f! a" A- A& y4 z$ C/ J* v6 O; @
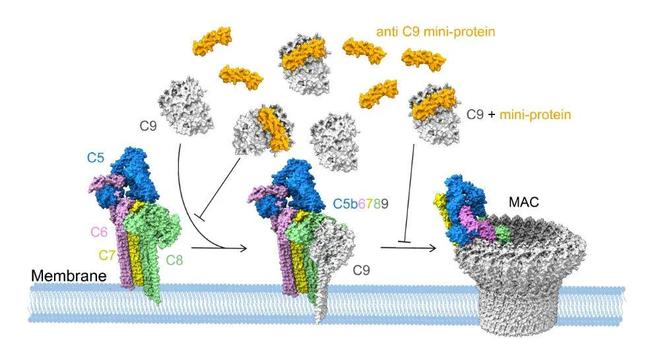
Design of miniprotEIn inhibitors targeting complement C9 to block membrane attack complex assembly 的研究论文。课题组基于深度学习算法从头设计了一类新型迷你蛋白抑制剂,该类抑制剂可有效阻断补体C9的膜插入过程并抑制其下游功能活性,阻断膜攻击复合物MAC形成,从而为干预补体系统异常活化相关疾病提供了创新性的治疗策略。(图1)。) D8 Z$ H" v+ j1 ~( d- h4 t
% e# y, F2 \. U

5 ~( q/ a j2 @/ B6 C
- ^3 R$ w! l4 X A
 6 [# I! o- l8 y8 l) T& ?* f4 s
6 [# I! o- l8 y8 l) T& ?* f4 s
& J0 M0 t% N8 O# a) X
图1 补体C9迷你蛋白抑制剂阻断膜攻击复合物形成的机制示意图) n0 w% u( s( I' v
随着AI扩散降噪、结构预测等技术的深度融合,蛋白质从头设计技术为补体介导的免疫系统疾病治疗开辟了全新路径,补体末端调控研究实现了从传统抗体研发向迷你蛋白抑制剂设计的转变。3 f, C( f! K6 s; O3 y& X+ s" T! y
尽管补体靶向治疗在阵发性睡眠性血红蛋白尿症(PNH)、非典型溶血性尿毒症综合征(aHUS)等疾病中已取得显著临床成效,但核心挑战依然存在:如何开发靶向补体C9的高效抑制剂,以实现对膜攻击复合物(MAC)组装的精准阻断,同时规避上游补体成分抑制所致的免疫功能受损等问题。补体C9作为MAC形成的终末关键组分,其功能界面呈现宽大、扁平且高度极性的结构特征,这为抑制剂的设计带来了挑战。然而,针对该靶点的精准阻断能够在补体级联反应启动后实现“刹车”作用,对急性溶血性疾病具有不可替代的应急治疗价值。
4 H, r |4 J, k) b6 c7 ]! N既往研究尝试通过单克隆抗体、细菌脂多糖等策略抑制C9聚合,但均存在明显局限:商业化抗C9单克隆抗体抑制活性微弱,且缺乏溶血性疾病治疗潜力的系统评估;脂多糖类抑制剂成药性差;传统抗体研发则面临C9功能界面高度保守导致的免疫筛选困难、热稳定性差以及生产工艺复杂、成本高昂等问题。此外,抗体分子量大、组织穿透性受限的特点,也使其在补体介导的局部组织炎症疾病中的应用受到制约。因此,开发靶向C9的迷你蛋白抑制剂成为该领域的关键科学问题。5 E g* ~3 \, }7 c; B
值得注意的是,既往补体抑制剂研发策略主要聚焦于补体上游成分(如C5)或依赖天然蛋白改造。前者会抑制C5a介导的天然免疫功能,增加感染风险,且部分患者因C5基因多态性存在治疗不敏感现象;后者则受限于天然蛋白的结构特征,难以实现对C9膜插入功能的精准阻断。因此,从头设计靶向补体C9的迷你蛋白抑制剂,需要突破C9扁平功能界面的设计瓶颈,同时兼顾抑制剂的高亲和力、高特异性、优异动力学特性及良好成药性。通过深度学习技术生成靶向补体C9功能界面的蛋白骨架,实现序列设计与复合物结构的精准匹配,在有效阻断C9膜插入和聚合的同时,确保抑制剂具备良好的可溶性、高表达量及热稳定性。% K( c% A) R$ |% ~
针对上述挑战,于博文、梁淑娟课题组联合研究了一类整合深度学习、扩散建模与功能实验验证的靶向补体C9迷你蛋白。该研究采用RFdiffusion进行蛋白骨架生成、ProteinMPNN进行序列设计,并结合AlphaFold2/3进行复合物结构预测,以补体C9的疏水热点区域为设计靶点,实现了对C9膜插入功能界面的精准靶向。通过部分扩散技术进一步优化抑制剂的结合亲和力,最终获得了高活性的靶向补体C9迷你蛋白抑制剂。经体外溶血抑制实验、蛋白互作检测及体内急性溶血模型验证,成功筛选出结构和功能优异的迷你蛋白抑制剂P9,P57。
+ l7 O" q4 a9 I, W2 ] n这些靶向补体C9的迷你蛋白抑制剂展现出优异的生物学特性:能够在补体级联反应启动后高效阻断MAC形成。其中,优化后的P9与人源C9的结合亲和力达到700 pM;在急性溶血模型中,即使于补体激活8分钟后给药,仍能实现几乎完全的溶血抑制,相较临床C5抑制剂依库珠单抗(Eculizumab)展现出更宽广的治疗窗口。这些迷你蛋白抑制剂由80-130个氨基酸残基构成,分子量小,可在大肠杆菌中实现高效表达——未经优化的摇瓶培养条件下,P9表达量达49.98 mg/L,P57达126.85 mg/L。此外,这些从头设计的迷你蛋白抑制剂具有极强的热稳定性:经95°C加热处理后冷却,仍能较大程度上恢复其二级结构并保留抑制活性。同时,其对C9具有高度特异性,不与C3、C4、C5、C6、C7、C8等其他补体组分发生交叉反应。3 | K* i! M) C9 P* w$ Y. Q
本研究进一步将设计的靶向补体C9迷你蛋白抑制剂应用于多种补体介导的溶血模型,包括小鼠血清介导的体外溶血、人血清介导的体外溶血、ABO血型不相容性溶血模型及小鼠体内血管内急性溶血模型等,均展现出高效的溶血抑制效果。此外,研究团队还将该迷你蛋白抑制剂应用于不同物种补体C9的跨物种抑制研究,成功筛选出对豚鼠、兔补体系统均具有抑制活性的候选抑制剂,为开发跨物种的补体抑制剂研究工具及临床前动物模型奠定了基础。$ V6 a7 P) ~6 [( [
通过一套整合深度学习、扩散建模与功能实验验证的计算蛋白设计方法,本研究首次从头设计出靶向补体C9的高活性迷你蛋白抑制剂,并从急性溶血疾病治疗、跨物种补体抑制等方向验证了其广泛的应用潜力。这项研究的意义不仅在于突破了C9扁平且极性功能界面的设计瓶颈,获得一系列结构新颖、性能优异的从头设计的补体C9抑制剂,为干预补体系统异常激活相关急慢性疾病提供了创新性的治疗策略;更重要的是为补体末端调控的蛋白-蛋白相互作用的从头设计提供了新的设计思路,为进一步从头设计靶向MAC组装的其他组分、构建可调控的补体干预分子奠定了坚实的基础。+ Q, Y7 A U7 N: M& ^) o2 c
山东第二医科大学于博文副教授,梁淑娟教授为本文的共同通讯作者。硕士研究生李敏,魏格格;高级实验师付晓燕,山东第二医科大学第一附属医院研究员王宁宁,西湖大学博士后张泽为本文的共同第一作者。
7 l1 O s2 Q% f文章链接:https://www.nature.com/articles/s41467-026-70667-x4 e9 i$ x6 a% s, }4 T3 N3 o% j
制版人: 十一
1 s! k3 v% M) F, }/ K. |8 H( S学术合作组织
0 {% p/ ]- \3 R) S! p7 @(*排名不分先后)1 e. \$ B L( R6 R! n
 n5 F7 A: O I
n5 F7 A: O I
& r2 g0 i* o" {7 q" s8 [( _* g2 p
/ m9 T! Z. |( ^9 C战略合作伙伴
; Q4 o) r$ u \8 m(*排名不分先后); Z( ?' e3 ` G+ g+ B

" B8 ~+ K4 H; K/ `8 r3 f: y% ]
, X# }% ]* W5 P4 C5 U6 q! U) u9 N! {
 1 t4 C# h' J3 v2 h0 Z% J
1 t4 C# h' J3 v2 h0 Z% J
6 i- Q! X1 ]$ K( ?5 i8 |7 t
转载须知
/ Y# R+ D3 P& w7 U. p
* O* s- D! b, H) x8 A【非原创文章】本文著作权归文章作者所有,欢迎个人转发分享,未经作者的允许禁止转载,作者拥有所有法定权利,违者必究。
5 J) s" r4 }6 ~5 e" X% GBioArt
3 f; l2 S4 f. G5 V0 C* \) GMed
9 g K2 m$ j0 `$ D, v( H" wPlants
/ `7 S! _6 J' C- Z; G# Q( |- |# A人才招聘/ W( r- f# f9 I3 w4 a$ G! n
近期直播推荐1 Z' L S+ U# e

0 p5 i: Y7 [- J) P2 J: X* z3 j3 h0 c; G4 A/ w
点击主页推荐活动, n, d5 y8 V7 p2 @. `
6 |2 O L, a. r; {. t4 o
关注更多最新活动!* r4 n( B& E# |4 V# t" S# o, v, y- P
# p) Q; h, L; I5 V+ ]9 _

|
|