|
|
 2 `; `. B3 p3 {2 E6 n5 C3 _
2 `; `. B3 p3 {2 E6 n5 C3 _
0 s* ~; @, x1 M. I* [沙门菌是重要的肠道病原菌,能够入侵并利用巨噬细胞作为复制场所【1】,但同时也需逃避巨噬细胞的吞噬清除【2】。血红素是细菌生长所需的重要铁源【3】,但其在病原菌与宿主免疫互作中的调控功能尚不明确。
% t5 f' P3 T Y$ Q% w2026年4月20 日 ,上海交通大学医学院姚玉峰、卢捷团队 在Nature Microbiology期刊发表了题为Salmonella-derived haem inhibits macrophage phagocytosis and promotes infection in mice的研究论文。该研究首次揭示沙门菌利用甲基转移酶SirM上调自身血红素合成,分泌的血红素作为通过TLR4-Cdc42信号轴抑制巨噬细胞的吞噬作用,同时诱导细胞焦亡,从而增强沙门菌在宿主体内的定植与致病能力。此外,SirM在多种肠道致病菌中高度保守,能帮助病原菌在与肠道共生菌的竞争中占据优势 。该研究揭示了病原菌利用代谢产物重塑宿主免疫微环境、实现免疫逃逸的新机制。$ x& ?3 F6 y1 ^) B1 s! _
 " Q% M0 u0 x2 j! I! z4 U7 O+ |
" Q% M0 u0 x2 j! I! z4 U7 O+ |
) P+ y& m. S8 _
为系统筛选肠道病原菌抵抗巨噬细胞吞噬作用的关键基因, 研究团队 以沙门菌为研究对象,利用 转座子测序 技术 ,首次鉴定出一个未知功能的甲基转移酶 基因,团队根据功能将其命名为 sirM ( S almonella i nternalization r egulator in m acrophages ) 。该 基因 在沙门菌与巨噬细胞接触后被显著激活, sirM 缺失株 更容易被 巨噬细胞吞噬,而回补 sirM 则可恢复 沙门菌 抗吞噬能力。. Z, ?4 `, S, |# G) u% S' p. o [
机制研究表明,SirM通过甲基化修饰血红素合成关键酶HemL,增强其酶活性,从而促进沙门菌血红素的合成与分泌。分泌至胞外的血红素 经 TLR4抑制Cdc42的激活,阻断巨噬细胞骨架重排和吞噬杯形成,进而抑制吞噬作用。与此同时,细菌来源的血红素与脂多糖协同作用, 促进 巨噬细胞焦亡,进一步破坏宿主免疫防御。小鼠 模型 实验证实, sirM 缺失株的毒力显著降低,小鼠存活率提高,组织病理损伤减轻,且细菌在脾、肝和粪便中的载量明显下降 ,表明SirM是沙门菌一种新型毒力因子 。
4 J( I' s' v$ j' p" y) v7 t# o令人关注的是,SirM及其介导的血红素合成机制在致病性肠杆菌科细菌( 如沙门菌、 致病性大肠杆菌 EHEC和EPEC )中高度保守,而在非致病性肠杆菌及肠道共生菌中缺失。竞争性感染实验表明,野生型沙门菌可有效逃逸巨噬细胞吞噬,并在与共生大肠杆菌的竞争中占据显著优势;而 sirM 缺失株则丧失这一优势。小鼠共感染模型进一步证实,SirM赋予沙门菌突破肠道定植抵抗的能力,从而在肠道炎症环境中建立有效感染。% q: d- ]1 M7 Y
 1 c8 q4 L Y! A7 G
1 c8 q4 L Y! A7 G
) Z- P' d: x2 {( A8 A
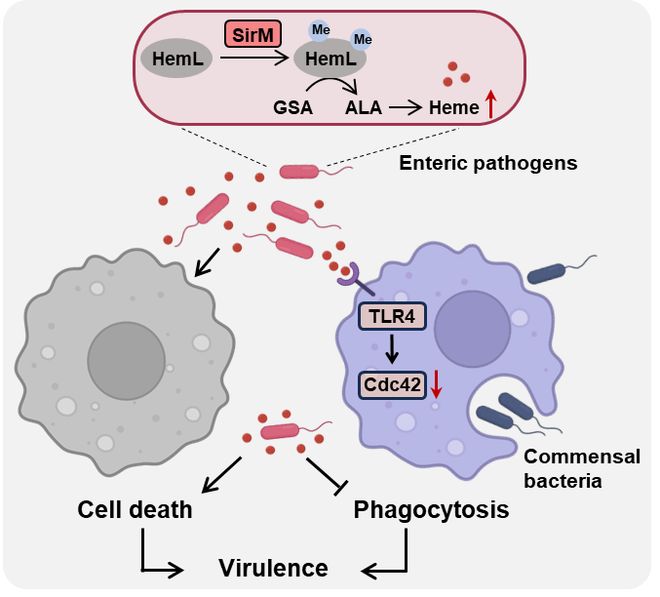
图1. 沙门菌甲基转移酶SirM作用机制
& q0 P0 @3 j" W. j# T该研究从病原菌视角出发,首次揭示了病原菌来源的血红素作为 自身代谢物 ,在逃逸宿主先天免疫应答中的 关键 作用。研究不仅深化了对病原菌-宿主互作机制的理解,也为开发靶向病原菌血红素合成/ 作用 途径的新型抗感染策略提供了理论基础和潜在药物靶点。6 t) t3 ` ~, T j
综上,该研究阐明了一条由细菌甲基转移酶SirM介导的血红素合成调控通路,揭示了病原菌利用代谢产物重塑宿主免疫反应、实现免疫逃逸并战胜肠道共生菌的独特策略,为干预肠道病原菌感染提供了新思路。
/ [& g6 f% v, i) p: ?上海市免疫学研究所博士后王佐强、直博生唐璜和黄婉秋为文章的共同第一作者,上海市免疫学研究所姚玉峰教授、上海交通大学医学院附属瑞金医院卢捷副研究员为文章的共同通讯作者。中国科学院分子植物科学卓越创新中心赵国屏院士,中国科学院上海市有机化学研究所潘李锋研究员,上海交通大学医学院许悦研究员,北京中医药大学张玫研究员,上海交通大学医学院附属仁济医院陈磊研究员,福建农林大学余道进教授 对本研究均有重要贡献。
7 _; N: L; t0 _. |' o姚玉峰 博士,上海交通大学医学院教授,上海市免疫学研究所 PI ,博士生导师,上海高校特聘教授,瑞金医院广慈教授。主要从事病原菌致病机制及宿主天然免疫研究,系统阐明了蛋白质翻译后修饰调控病原菌毒力相关双组分系统的分子机制,为相关靶向抗菌药物的研发提供了新的理论基础,并 为 Trends Microbiol 撰写特邀综述。 已经在Nat Microbiol、 Nat Commun 、 Cell Rep 、 PLoS Pathog 、 NAR 、 mBio 等国际知名期刊上发表研究论文 80 多篇。科研工作获得国家自然科学基金委重点项目、 NIH-NSFC 国际合作重点项目、面上项目、科技部 973 计划课题、重点研发专项、传染病重大专项和上海市科委、教委的资助。姚玉峰课题组长期招收博士后,具有微生物学和感染免疫等相关背景优先,欢迎更多优秀的人才(包括博士后等)加入。请感兴趣的申请者来函咨询。4 s! E, a& X: G: M( C! [
简历投递( 有意者请将个人简历等材料发至 ):
1 y2 b( n. c- Ghttps://jinshuju.net/f/ZqXwZt或扫描二维码投递简历7 h. n9 a, Z& U* `+ Q( M; u
https://www.nature.com/articles/s41564-026-02341-3: d8 v. K/ O. L# C u( i
制版人: 十一
* ]3 L4 a9 l. \/ Y. C1 j参考文献 H" w; E' t5 C
1 LaRock, D. L., Chaudhary, A. & Miller, S. I. Salmonellae interactions with host processes.Nat Rev Microbiol13, 191–205 (2015). https://doi.org/10.1038/nrmicro3420+ w, O3 j/ C- H: Q* l7 Y# L8 P
2 Brown, G. C. Cell death by phagocytosis.Nat Rev Immunol24, 91–102 (2024). https://doi.org/10.1038/s41577-023-00921-6
0 C* ?: J8 |; W& w* u3 s3 Contreras, H., Chim, N., Credali, A. & Goulding, C. W. Heme uptake in bacterial pathogens.Curr Opin Chem Biol19, 34–41 (2014). https://doi.org/10.1016/j.cbpa.2013.12.014% ~; O! W% R+ Y2 g5 L
学术合作组织
, f& R6 G9 L$ I2 }(*排名不分先后)
$ K7 }7 M9 N7 `0 r! s) G9 O/ P

4 V! t0 [" f$ N Y- `0 l4 }) P) o
/ @) b9 t5 N5 `2 \/ u
Q- P- e. b4 e" U战略合作伙伴/ E* \" C8 ?6 W6 j3 c! {$ O
(*排名不分先后)
; Y( O o% `/ s& w+ Z) C p; f

$ G/ X( M: R! E8 Y/ b( p& v1 O1 k. c7 l' w; x. d8 c
 9 [# A2 _" B; m5 k+ K$ o8 Z" s
9 [# A2 _" B; m5 k+ K$ o8 Z" s
8 F0 X# w H R$ U G转载须知: L, P5 c, o' f- f
$ W; P9 Y( @4 D ~ E; B# n0 J. ^# _ X
【非原创文章】本文著作权归文章作者所有,欢迎个人转发分享,未经作者的允许禁止转载,作者拥有所有法定权利,违者必究。
. b$ R9 a9 N1 v0 q2 x' X5 [% vBioArt
% w) p, ]3 {, E' U6 J/ vMed
2 U j7 D6 n0 b9 t: T+ Z' `( }Plants+ r2 T/ h! G6 _5 c: s ^1 |# ?
人才招聘
2 K8 l+ t% F9 G
 ' R6 d. t- k$ t. l
' R6 d. t- k$ t. l
0 e7 C f7 I8 Q$ X1 U; s. R点击主页推荐活动
, m, a- ]0 a. F- l) r5 {) H5 W( r+ j! a& W9 Y) Y
关注更多最新活动!
" P; b E! i4 _. r- F/ X: l1 X2 T
/ f6 S6 y9 K& q* V2 u& n# D

|
|