|
|
全球超过2600万人受到先天性听力损失影响,其中约60%病例由遗传因素导致。
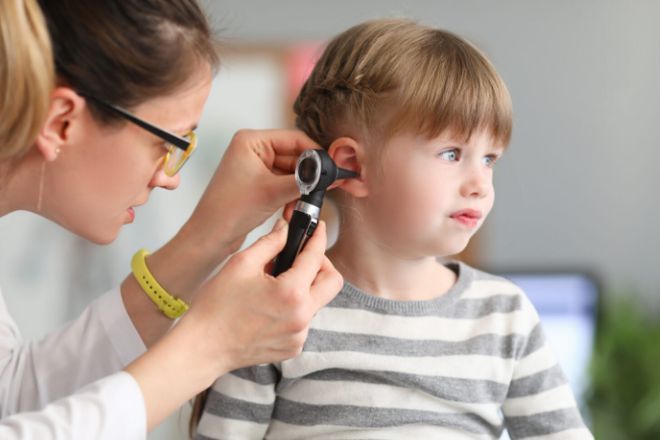
: ]# C5 p" i; k8 B0 g \! q( _DFNB9型耳聋,由OTOF基因突变引起,是一种常染色体隐性遗传疾病。突变导致Otoferlin蛋白异常,它在内耳毛细胞中负责将声音信号传递至大脑,是孩子正常听力和语言发育不可或缺的“信号桥”。
, Q( k& q1 E! L- g T) A! Y. W$ W) s
 ! v) A& H9 M7 U2 _% a0 C$ X5 z) n, l
! v) A& H9 M7 U2 _% a0 C$ X5 z) n, l
5 R2 Z9 x# N7 Q1 Z, |6 T! A" r
- J9 q+ Q" ]# S0 ]缺失或异常的Otoferlin让孩子无法听到声音,也难以正常发育语言,人工耳蜗虽能部分辅助,但复杂噪声环境下理解能力仍有限。7 r. p" Q; {9 v* N
在这种背景下,科学界迫切需要一种能够直接纠正基因缺陷、恢复听力的根本性方案。
* i) @ R2 c$ n+ |' h" V此前尝试仅局限于药物、手术或辅助器械,无法从分子层面改变疾病进程。国际上,AAV(腺相关病毒)载体因安全性高、能靶向内耳毛细胞而被视为理想基因载体,为先天性耳聋基因治疗提供新契机。- n7 C8 C$ a9 q2 u2 s) p8 Z2 d' r9 @
01、OTOF基因与听力的分子密码
. z X3 [& L- Q' a' T2 @ xDFNB9型耳聋的核心在于OTOF基因突变。Otoferlin蛋白像一个“信号开关”,将机械振动转换为神经冲动传递给大脑。如果开关失灵,声音无法识别,孩子听不到语言,也难以在噪声环境中理解声音。9 x& T, X. W( c" [, H& Z, P
OTOF突变类型多样,包括点突变、缺失或移码突变,但其病理机制一致——阻断毛细胞与听神经之间的信号通路。由于缺陷直接作用于听觉信号传递,传统药物无法解决问题,因此基因治疗成为首选。
4 P/ n: O" }. @4 s: C0 C临床上,患者通常在婴幼儿期就表现听力缺失,若错过早期干预,语言学习和社会适应能力恢复难度大幅增加。; U% H* J9 K# ]1 ^. L
02、AAV基因治疗——把声音带回孩子的世界+ t5 k V2 A$ u
2026年4月22日,复旦大学附属眼耳鼻喉科医院联合哈佛大学医学院团队在《Nature》发表研究,首次系统报道多中心AAV基因治疗DFNB9型耳聋的临床试验。
, O# u6 g" b _4 f4 p
 & G% V! I$ l5 M. \
& G% V! I$ l5 M. \
% L1 c% b- r, E
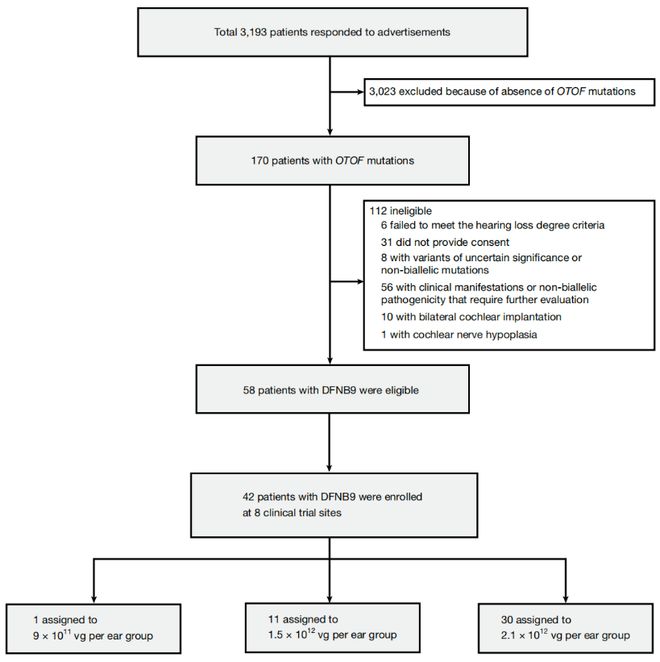
8 a3 Y! t, F0 F3 L研究共纳入42名患者,年龄从9个月至32岁,覆盖婴幼儿、儿童、青少年和成年人,是该领域年龄跨度最广的研究。患者被分为三个剂量组,接受单耳或双耳注射。! o/ R8 A) Q3 P2 a4 N; W
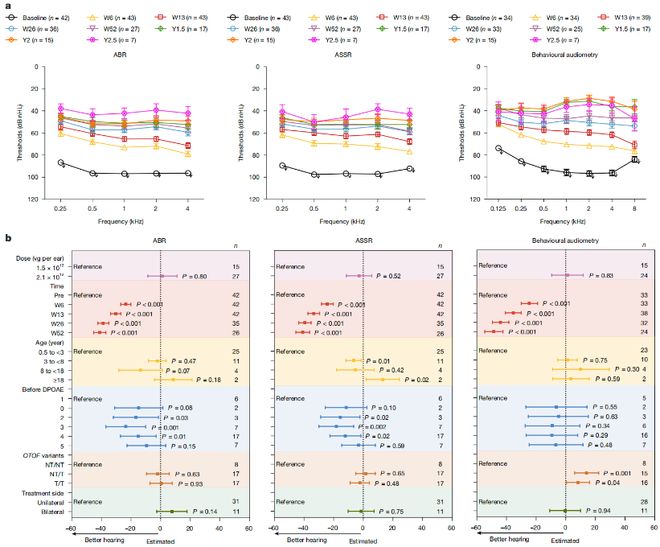
3 {, G( J: R/ F: r▲基因治疗后患者听力恢复情况的听力测试结果/ A' m ?: ^# E2 G1 t9 G: ^ \
Y, }/ }. i) T+ l
治疗后,90%患者听力显著改善,效果稳定持续至最长2.5年随访期。成年患者也获益:3名20岁以上患者中,2人(20岁和32岁)听力明显恢复,证实基因疗法对成年耳聋患者也有效。8 A8 A1 g% z/ r+ B: @% O) n
数据表明,越早干预、毛细胞尚未退化、剂量适中,疗效越佳,为全球耳聋患者提供新希望。0 f" V2 B! D* ]* C7 O
03、多中心试验的真实数据! n( b! A! Y, Q3 }: T
研究显示,AAV基因治疗可显著改善声音感知和言语理解能力。受试者在安静环境中平均听力恢复达85–95分贝,部分患者在噪声环境中理解能力也提升。多中心设计涵盖复旦、北京协和、南方大学附属医院及哈佛医学院,使结果更具代表性。
# ?6 Z( G" n1 U' Q# O% h5 H各剂量组疗效存在差异:低剂量组主要改善基础听力,中高剂量组在言语理解和噪声环境分辨能力上表现更佳。此外,双耳注射患者在复杂环境下的理解能力更突出,为今后个体化治疗提供科学依据。
; \& M* B& \+ l6 y2 J' l04、国际视角与疗效规律——谁最能受益. X5 m% v/ Z& r
根据试验数据,治疗效果与年龄、剂量和注射策略密切相关。总体来看,婴幼儿和儿童疗效最佳,早期干预可让毛细胞在尚未退化状态下恢复功能,听力和语言改善最明显。
& E7 o. @: [# L0 H) H! N青少年和成年患者也可获益,但相对改善幅度略低。剂量方面,中高剂量组在声音感知和言语理解上表现更好,低剂量组主要改善基础听力。
& m/ U6 ^- A3 J+ T* E- v" q注射策略也影响疗效:双耳注射患者在复杂环境下言语理解能力更突出。值得振奋的是,3名20岁以上成年患者中,有2人听力明显恢复,表明成年患者仍可受益。
* p: T( e, K' ]% d总的来说,越早治疗、毛细胞未退化、剂量适中、注射策略优化的患者听力恢复效果最佳,为未来个体化基因治疗提供科学依据。
$ D6 o% s2 Q3 d/ j: V/ a4 p! j05、声音重生——基因让孩子拥抱世界
, F' M. g* |. K8 y$ m. H/ j这一突破不仅是科研胜利,更是全球先天性耳聋患者的新希望。4 q/ C4 Z8 [. [$ ^, f
通过AAV基因治疗,声音再次进入孩子世界,他们能听到父母呼唤、感受音乐韵律,语言能力得以正常发育。随着技术推广与国际合作,这种治疗模式有望成为全球标准,为遗传性耳聋患者提供可靠、长期干预方案。9 V# R, W+ Z) R" E! H) L
正如研究团队所言:“用分子级干预让孩子听见世界,是医学与科技交织的最美实践。”$ b& g* X; h' B* g7 D% b
文献来源:
1 r; p0 N/ v( \7 z2 p1 EMulticentre gene therapy forOTOF-related deafness followed up to 2.5 years
& a5 b5 v+ U* g* |7 I4 t& S" G2 {Luoying Jiang, Xiaoting Cheng, Jun Lv......
9 L' t" l& U0 \* U4 e' bDOI: 10.1038/s41586‑026‑10393‑y |
|