|
|
来源:市场资讯
5 ]5 {) V) x( M- w(来源:药时空)
9 g: P N7 K9 P5 [5 L2 A手足口病是严重威胁儿童健康的重要传染病。近年来,柯萨奇病毒A6型(CVA6)已取代肠道病毒EV-A71,成为手足口病的主要病原体之一,且常导致非典型症状甚至重症。然而,决定CVA6强致病性的关键病毒因子长期不明,也尚无获批的疫苗或特效药物。
4 S5 ]0 L8 _) W* p8 c+ }! ]# a近期,上海市重大传染病和生物安全研究院张超课题组在国际病毒学权威期刊 Journal of Virology 上在线发表了题为“A single residue in the VP3 capsid protEIn governs virulence and informs live-attenuated vaccine design for coxsackievirus A6”的研究论文。该论文因其重要价值被期刊编辑选为本期 Editor's Pick(编辑精选)。研究首次鉴定出VP3衣壳蛋白第238位氨基酸是决定CVA6致病性的关键分子开关,并基于此机制理性设计了一种高效、安全的减毒活疫苗候选株。
1 G' ~" \) r* g% O' C. }

: B' o' J1 n5 V% p( U) `
2 g. o( U) T/ h3 V/ J& ^系列重要发现1/ q, u0 k0 p0 q! ^) E
毒力分子开关的鉴定:从P1区到单个氨基酸,并印证其在自然界的优势- |! `" J! ~" i- Z" e
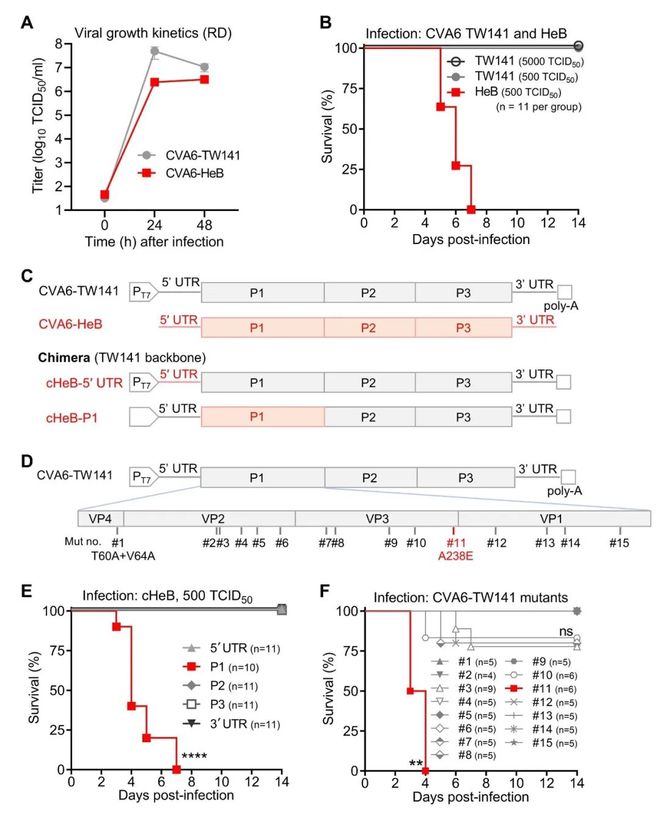
研究首先发现,临床分离株CVA6‑HeB(河北株)与感染性克隆拯救的CVA6‑TW141(台湾株)在体外培养细胞中具有相似的复制动力学(图1A),但在新生乳鼠中的致病性却截然不同:CVA6‑HeB可导致100%死亡,而CVA6‑TW141即使在高剂量下也不引起死亡和严重疾病(图1B)。; n3 L/ L5 ^3 D) y; x( j
为定位毒力决定区域,研究者在非致死的CVA6‑TW141骨架上构建了一系列嵌合病毒,分别替换CVA6‑HeB的不同基因组片段(图1C)。乳鼠感染实验表明,只有携带CVA6‑HeB来源P1区(衣壳蛋白编码区)的嵌合病毒获得了完全的致死能力,而其他嵌合病毒均不致死(图1E),从而将毒力决定区域精确锁定在P1衣壳区。
! ? ~1 A7 ~, G) H) aCVA6‑HeB与CVA6‑TW141的P1区共有19个氨基酸差异。为进一步精确定位关键位点,研究者在CVA6‑TW141骨架上逐一引入这些差异位点,构建了15株点突变病毒(图1D)。乳鼠感染筛选发现,仅引入VP3‑A238E突变(即将弱毒株的VP3蛋白238位丙氨酸A突变为强毒株的谷氨酸E; #11突变体)即可使原本无害的CVA6‑TW141获得100%的致死能力(图1F)。反之,在致死性嵌合病毒中将VP3‑E238突变回丙氨酸(E238A),则可完全消除其致死性。这些结果证明,VP3第238位氨基酸是决定CVA6致病性的充分必要条件:E(谷氨酸)赋予强毒力,A(丙氨酸)导致完全减毒。( k( _' X7 f2 q
对NCBI数据库中1,276条CVA6 VP3序列的分析显示,谷氨酸(E)在第238位占绝对主导地位(>93%),而丙氨酸(A)及其他天然变异则极为罕见。功能验证表明,在所有天然变异中,只有E238能够赋予病毒完全的致死能力,其他变异即使在高剂量下也仅引起部分致死。这表明VP3‑E238是自然界中CVA6高毒力流行株的关键分子基础,也为疫苗设计提供了精确的靶点。; h* k! p$ s. i/ b( g- c
 ; X& N, ^0 {, J: {5 U
; X& N, ^0 {, J: {5 U
7 v2 ]1 O, c; V5 i' X! w系列重要发现2
3 y7 d% w. D" k减毒机制:削弱受体结合而非破坏病毒基本特性
- k7 m, a! R3 B- s6 ?E238A突变并不影响病毒的体外基本特性。纯化的E238A突变病毒与野生型病毒具有相似的颗粒形态、抗原性、感染性及细胞吸附能力(图2A-D)。然而,在乳鼠体内,E238A突变显著降低了病毒在靶组织(尤其是脊髓和肢体肌肉)中的复制能力,组织病理损伤明显减轻,毒力降低超过10,000倍(图2E-F)。( ~' m1 Y3 Q# F' U( t8 x: a
机制研究发现VP3‑E238位于病毒表面“峡谷”(canyon)区的边缘(图2G),该区域是病毒与主要受体KREMEN1结合的关键部位。E238A突变显著削弱了病毒与鼠源KREMEN1受体的结合能力(图2H),这解释了该突变导致体内复制受限和毒力减弱的分子机制。
$ l* I% ?" p2 m1 @6 Z6 N6 o7 D' P9 L0 \) |值得一提的是,我们此前在Nature Communications(2025)上系统阐明了CVA6采用“硫酸乙酰肝素附着‑KREMEN1脱衣壳”的双受体入侵模型,并证明KREMEN1能高效诱导成熟病毒颗粒发生构象转变。 本研究中VP3‑E238对KREMEN1结合的调控作用,进一步深化了对该受体介导CVA6病毒入侵分子细节的理解。0 T" P: Y u5 m* `! Q# x2 n
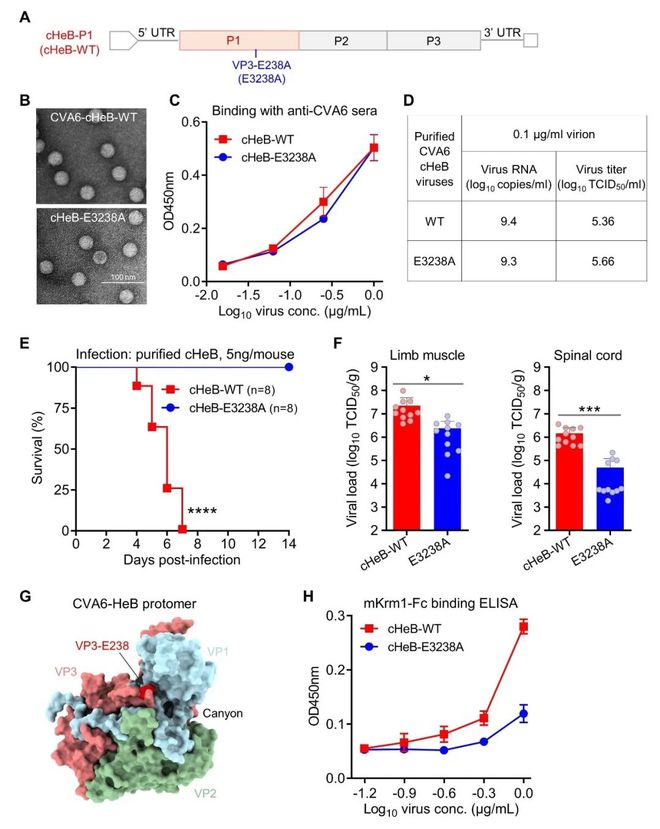
" G; s6 \3 y# d& S s图2. CVA6 VP3-E238A突变导致体内毒力显著减弱的分子机制。
$ }, Y0 e3 A, M0 t6 T( E; S1 \: ? A* g9 C: B6 J; u
系列重要发现3
, ~5 o4 K8 B6 t' E# w从机制到应用:一款高效的CVA6减毒活疫苗候选株+ z/ S7 I5 {2 e& R
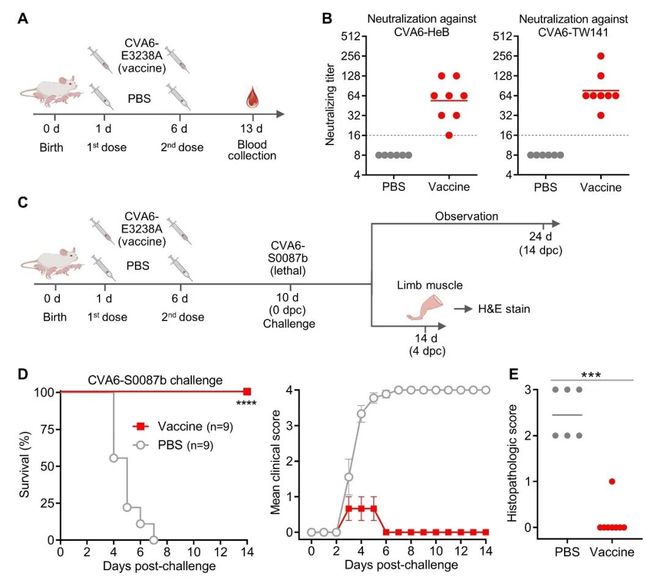
基于上述发现,研究者将VP3-E238A突变引入CVA6‑HeB衣壳骨架(该骨架以成熟病毒颗粒为主,免疫原性更优),构建了减毒活疫苗候选株cHeB‑E3238A。该疫苗株在乳鼠中完全减毒,但保留了良好的免疫原性。两剂免疫后,所有小鼠均产生了中和抗体(图3A-B)。随后,研究者采用一株异源的、高度致死的CVA6‑S0087b毒株进行攻击,攻毒剂量高达93,545个LD50。结果显示,疫苗免疫组获得100%保护,而对照组全部死亡(图3C-D)。组织病理学分析进一步证实,疫苗免疫显著减轻了攻击后的肌肉损伤(图3E)。此外,遗传稳定性分析显示,E238A突变在乳鼠肌肉复制后短期未发生回复突变,为疫苗的安全性提供了初步证据。. ?4 o, H8 k8 I- k
 , t. S& k& z; M) \( M M" i
, t. S& k& z; M) \( M M" i
图3. CVA6减毒活疫苗候选株cHeB‑E3238A的体内保护效果的验证。. w6 @& v8 n3 M" w
9 [! c9 ^. a) p; n8 C综上所述,本研究首次鉴定出VP3第238位氨基酸是决定CVA6致病性的关键分子开关,揭示了其通过调控KREMEN1受体结合影响体内复制和致病力的分子机制。更重要的是,基于这一发现理性设计的减毒活疫苗候选株在乳鼠模型中表现出了良好的安全性和保护效力,为CVA6疫苗的研发提供了全新的策略。
9 C; A- t# Q$ E5 [' V0 f上海市重大传染病和生物安全研究院硕士研究生刘可歆为本文第一作者,张超青年研究员为唯一通讯作者。该研究得到了中国疾病预防控制中心张勇研究员、厦门大学程通教授、浙江大学番文春研究员、中国科学院蓝佳明研究员等人的帮助。研究获得了国家重点研发计划、上海市市级科技重大专项、国家高层次人才计划的资助。 |
|